Tìm hiểu phản ứng este hóa là gì?
Định nghĩa phản ứng este hóa là gì?
Phản ứng este hóa được biết đến là phản ứng giữa axit cacboxylic và ancol trong điều kiện nhiệt độ, có \(H_2SO_4 \)đặc làm xúc tác. Trong điều kiện đó, đồng thời xảy ra phản ứng thủy phân este trong môi trường axit, tạo ra axit và ancol ban đầu. Phản ứng este hóa và phản ứng thủy phân este trong axit là phản ứng thuận nghịch, hiệu suất phản ứng H <100%.
Phương trình tổng quát phản ứng este hóa
\(R(COOH)_{x} + R'(OH)_{t} \rightleftharpoons Ry(COO)_{xy}R’_{x} + xyH_{2}O\) (xúc tác \(H_2SO_4 \) ,\(t^0\))
- Nếu axit cacboxylic và ancol tham gia phản ứng đều thuộc loại đơn chức (hay gặp) thì phản ứng có phương trình dạng:
\(RCOOH + R’OH \rightleftharpoons RCOOH + H_{2}O\) (xúc tác \(H_2SO_4 \) ,\(t^0\))
- \(H_2SO_4 \)đặc trong phản ứng này ngoài vai trò là xúc tác của phản ứng còn làm nhiệm vụ hút nước.
Hiệu suất phản ứng este hóa
Bài toán hiệu suất thuận
- Đề bài cho số liệu của chất tham gia phản ứng, yêu cầu đi tìm các chất tạo thành (sản phẩm).
- Công thức tính:H% = \(\frac{m_{tt}}{m_{lt}}.100\)
- hoặc H% = \(\frac{n_{pu}}{m_{bd}}.100\)
- Luôn luôn lấy số liệu của sản phẩm để tính cho bài toán
- Nếu bài toán cho hiệu suất thì sau khi tính toán chỉ cần nhân với hiệu suất suy ra kết quả cần tìm.
Bài toán hiệu suất nghịch
- Đề bài cho số liệu sản phẩm, yêu cầu tính khối lượng các chất tham gia phản ứng
- Công thức tính: H% = \(\frac{m_{tt}}{m_{lt}}.100\)
- hoặc H% = \(\frac{n_{pu}}{m_{bd}}.100\)
Lưu ý:
- Nếu bài toán đã cho hiệu suất thì sau khi tính toán xong chỉ cần chia kết quả cho hiệu suất suy ra kết quả cần tìm
- Khi đề bài cho chất tham gia ban đầu có chứa bao nhiêu phần trăm tạp chất \(⇒ \)lượng chất tham gia thực tế = lượng chất cho trong đề.(100 – % tạp chất.
- Đề bài cho sự hao hụt trong quá trình phản ứng/sản xuất thì lượng chất thực tế phản ứng = lượng chất trong đề bài.(100% – % hao hụt).
- Hiệu suất tính theo chất dư ít hơn.
- Khi đề bài cho quá trình gồm n giai đoạn, mỗi giai đoạn có hiệu suất \(H_{1},H_{2},…,H_{n},…\)thì hiệu suất của toàn quá trình là \(H = H_{1}.H_{2}….H_{n}\)
Phản ứng xà phòng hóa este
- Phản ứng xà phòng hóa là quá trình thủy phân este trong môi trường kiềm, tạo thành ancol và muối cacboxylat.
- Phản ứng xà phòng hóa là phản ứng 1 chiều, nhưng phản ứng có thể xảy ra hoàn toàn hoặc không hoàn toàn. Hiệu suất phản ứng \(H\leq 1\), \(H = 1\): phản ứng xảy ra hoàn toàn.
Phương trình tổng quát
\(R_{y}(COO)_{xy}R’_{x} + xyNaOH \rightarrow y(COONA)_{x} + R'(OH)_{y}\)
\(m_{chat\, ran \, sau\, phan \, ung} = m_{muoi} + m_{kiem du}\)
Với este đơn chức: \(n_{este \, phan\, ung} = n_{NaOH\, phan\, ung} = n_{muoi} = n_{ancol}\)
Xem chi tiết >>> Phản ứng xà phòng hóa: Lý thuyết và Bài tập ứng dụng
Bài tập phản ứng este hóa và phương pháp giải
Dạng 1: Tính hằng số cân bằng
Phương pháp tính hằng số cân bằng
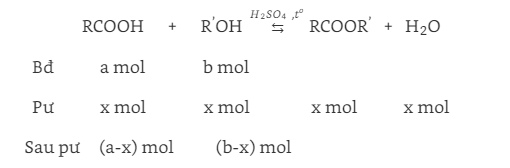
\(K_{C} = \frac{\left [ RCOOR’ \right ]\left [ H_{2}O \right ]}{\left [ RCOOH \right ]\left [ R’OH \right ]} = \frac{\frac{x}{V} . \frac{x}{V}}{\frac{a-x}{V}.\frac{b-x}{V}} = \frac{x^2}{(a-x)(b-x)}\)
Ví dụ 1: Cho biết hằng số cân bằng của phản ứng este hóa: \(R-COOH + R’OH \rightleftharpoons R-COOR’ + H_{2}O\) có \(K_C=4\). Nếu cho hỗn hợp cùng số mol axit và ancol tác dụng với nhau thì khi phản ứng este hóa đạt tới trạng thái cân bằng thì có bao nhiêu phần trăm ancol và axit đã bị este hóa?
Giải:
Ta có:
\(\left [ R_{1} COOR_{2} \right ] = \left [ H_{2}O \right ] = x\)
\(\left [ R_{1} COOH \right ] = \left [ R_{2}OH \right ] = a – x\)
\(K_{C} = \frac{\left [ R_{1}COOR_{2} \right ].\left [ H_{2}O \right ]}{\left [ R_{1}COOH \right ].\left [ R_{2}OH \right ]} = \frac{x^2}{(a – x)^2} = 4\)
\(\Rightarrow x = 2(a – x) \Leftrightarrow 3x = 2a \Rightarrow \frac{x}{a} = \frac{2}{3} = 0,667\)
Vậy khi phản ứng este hóa đạt tới trạng thái cân bằng thì có 66,67% ancol và axit đã bị este hóa.
Dạng 2: Tính hiệu suất của phản ứng este hóa
- Phương pháp tính hiệu suất phản ứng este hóa
Nếu \(a\geq b \Rightarrow H = \frac{x}{b}.100 \Rightarrow x = \frac{H.b}{100};\, b = \frac{100.x}{H}\)
Nếu \(a < b \Rightarrow H = \frac{x}{a}.100 \Rightarrow x = \frac{H.a}{100};\, a = \frac{100.x}{H}\)
- Phương pháp giải nhanh:
Áp dụng định luật bảo toàn khối lượng: \(m_{ancol} + m_{axit} = m_{este} + m_{nuoc}\)
Hiệu suất phản ứng este hóa \(H = \frac{m_{este\, TT}}{m_{este\, LT}}.100\)
Ví dụ 2: Thực hiện phản ứng este hóa 9,2g glixerol với 60g axit axetic. Giả sử chỉ thu được glixerol triaxetat có khối lượng 17,44g. Tính hiệu suất của phản ứng este hóa.
Giải:
\(n_{glixerol} = 0,1\, mol\)
\(n_{axit\, axetic} = 1\, mol\)
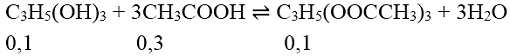
Từ pt: \(m_{este} = 0,1.218 = 21,8g\)
Thực tế: \(m_{este} = 17,44g\)
Hiệu suất: H% = \(\frac{17,44}{21,8}.100 = 80\)
Như vậy, Phản ứng este hóa là gì? Hiệu suất phản ứng este hóa? Đặc điểm của phản ứng este hóa? Phản ứng xà phòng hóa este? Phản ứng este hóa giữa ancol etylic và axit axetic? Bài tập phản ứng este hóa lớp 9? đều được Dinhnghia.vn giải đáp trong bài viết trên. Hy vọng đã cung cấp cho bạn những kiến thức hữu ích phục vụ quá trình nghiên cứu và học tập nói chung cũng như tìm hiểu về phản ứng este hóa là gì nói riêng. Chúc bạn luôn học tốt!
Xem thêm >>> Phản ứng nhiệt nhôm là gì? Các phản ứng nhiệt nhôm thường gặp
Xem thêm >>> Phản ứng oxi hóa khử là gì? Ví dụ phương trình phản ứng oxi hóa khử
Xem thêm >>> Phản ứng hữu cơ là gì? Cơ chế, Lý thuyết và Bài tập