Canxi oxit (CaO) là gì?
Tính chất vật lý của CaO
- Là chất rắn màu trắng, nóng chảy ở nhiệt độ rất cao (\(2585^{\circ}C\))
- Canxi oxit có đầy đủ tính chất của một oxit bazơ.
Tính chất hóa học của CaO
CaO (vối sống) là một oxit bazơ tan trong nước và phản ứng với nước, có những tính chất hóa học sau:
- Tác dụng với nước:
\(CaO + H_{2}O \rightarrow Ca(OH)_{2}\)
Phản ứng của canxi oxit với nước gọi là phản ứng tôi vôi, chất \(Ca(OH)_{2}\) tạo thành gọi là vôi tôi, là chất rắn màu trắng, ít tan trong nước, phần tan tạo thành dung dịch bazơ còn gọi là nước vôi trong.
- Tác dụng với axit tạo thành muối và nước.
Ví dụ:
\(CaO + 2HCl \rightarrow CaCl_{2} + H_{2}O\)
- Tác dụng với oxit axit tạo thành muối.
Ví dụ:
\(CaO + CO_{2} \rightarrow CaCO_{3}\)
Ứng dụng của canxi oxit (CaO)
CaO có những ứng dụng chủ yếu sau đây:
- Phần lớn canxi oxit CaO được dùng trong công nghiệp luyện kim và làm nguyên liệu cho công nghiệp hóa học.
- Canxi oxit CaO còn được dùng để khử chua đất trồng trọt, xử lí nước thải công nghiệp, sát trùng, diệt nấm, khử độc môi trường,…
- Canxi oxit CaO có tính hút ẩm mạnh nên được dùng để làm khô nhiều chất.
Sản xuất canxi oxit (CaO) trong công nghiệp
Nguyên liệu để sản xuất canxi oxit là đá vôi (chứa \(CaCO_{3}\)). Chất đốt là than đá, củi, dầu, khí tự nhiên,…
Các phản ứng hóa học xảy ra khi nung vôi:
- Than cháy sinh ra khí \(CO_{2}\)và tỏa nhiều nhiệt
\(C + O_{2} \rightarrow CO_{2}\)
Nhiệt sinh ra phân hủy đá vôi ở khoảng trên \(900^{\circ}C\)
\(CaCO_{3} \rightarrow CaO + CO_{2}\)
Lưu huỳnh đioxit (\(SO_{2}\)) là gì?
Tính chất vật lí của \(SO_{2}\)
Lưu huỳnh đioxit là chất khí không màu, mùi hắc, độc (gây ho, viêm đường hô hấp…), nặng hơn không khí.
Tính chất hóa học của \(SO_{2}\)
Lưu huỳnh đioxit là một oxit axit tan trong nước và phản ứng với nước, có những tính chất hóa học sau:
- Tác dụng với nước tạo thành dung dịch axit:
\(SO_{2} + H_{2}O \rightarrow H_{2}SO_{3}\) (axit sunfurơ)
\(SO_{2}\) là chất gây ô nhiễm không khí, là một trong các chất gây ra mưa axit.
- Tác dụng với dung dịch bazơ tạo thành muối và nước:
Ví dụ:
\(SO_{2} + Ca(OH)_{2} \rightarrow CaSO_{3} + H_{2}O\)
Khi \(SO_{2}\)tác dụng với dung dịch bazơ có thể tạo muối trung hòa và muối axit.
- Tác dụng với oxit bazơ (tan) tạo thành muối:
Ví dụ:
\(SO_{2} + Na_{2}O \rightarrow Na_{2}SO_{3}\)
Ứng dụng của lưu huỳnh đioxit (\(SO_{2}\))
- Phần lớn \(SO_{2}\) dùng để sản xuất axit sunfuric \(H_{2}SO_{4}\).
- Dùng làm chất tẩy trắng bột gỗ trong sản xuất giấy, đường,…
- Dùng làm chất diệt nấm mốc,…
Điều chế lưu huỳnh đioxit (\(SO_{2}\))
- Trong phòng thí nghiệm
Cho muối sunfit tác dụng với axit mạnh như \(HCl,\)\(H_{2}SO_{4}\),…
Ví dụ:
\(Na_{2}SO_{3} + H_{2}SO_{4} \rightarrow Na_{2}SO_{4} + SO_{2} + H_{2}O\)
Khí \(SO_{2}\)được thu bằng phương pháp đẩy không khí.
- Trong công nghiệp
Đốt lưu huỳnh hoặc quặng pirit sắt \(FeS \)trong không khí:
\(S + O_{2} \rightarrow SO_{2}\)
\(4FeS_{2} + 11O_{2} \rightarrow 2Fe_{2}O_{3} + 8SO_{2}\)
Bài tập về một số oxit quan trọng
Bài 1: 200ml dung dịch HCl có nồng độ 3,5 mol/l hòa tan vừa đủ 20g hỗn hợp \(CuO \)và \(Fe_{2}O_{3}\)
- Viết các phương trình phản ứng hóa học.
- Tính khối lượng của mỗi oxit bazơ có trong hỗn hợp ban đầu.
Cách giải:
\(V_{HCl} = 200\, ml = 0,02\, l\)
\(n_{HCl} = 3,5.0,02 = 0,7\, (mol)\)
Gọi x, y là số mol của \(CuO \)và \(Fe_{2}O_{3}\)
- Phương trình phản ứng hóa học :
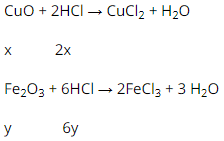
2. Từ phương trình phản ứng trên ta có:
\(n_{HCl}\, (1) = 2.n_{CuO} = 2x\, mol\)
\(n_{HCl}\, (2) = 6.n_{Fe2O3} = 6y\, mol\)
\(\Rightarrow n_{HCl} = 2x + 6y = 0,7\, mol\) *
\(m_{CuO} = (64 + 16).x = 80x\, g\)
\(m_{Fe_{2}O_{3}} = (56.2 + 16.3).y = 160y\, g\)
Theo bài:
\(m_{hh} = m_{CuO} + m_{Fe_{2}O_{3}} = 80x + 160y = 20g\)
\(\Rightarrow x + 2y = 0,25 \Rightarrow x = 0,25 – 2y\) (∗∗)
Thay x vào (∗) ta được:
2.(0,25 – 2y) + 6y = 0,7
⇒ 0,5 – 4y + 6y = 0,7
⇒ 2y = 0,2 ⇒ y = 0,1 mol
Thay y vào (∗∗) ta được:
x = 0,25 – 2.0,1 = 0,05 mol
\(\Rightarrow m_{CuO} = 0,05 . 80 = 4g\)
\(m_{Fe_{2}O_{3}} = 0,1.160 = 16g\)
Bài 2: Biết 2,24 lit khí \(CO_{2}\)(đktc) tác dụng vừa đủ với 200ml dung dịch \(Ba(OH)_{2}\) sản phẩm sinh ra là \(BaCO_{3}\)và \(H_{2}O\).
- Viết phương trình phản ứng.
- Tính nồng độ mol của dung dịch \(Ba(OH)_{2}\) đã dùng.
- Tính khối lượng chất kết tủa thu được.
Cách giải:
\(n_{CO_{2}} = \frac{V}{22,4} = \frac{2,24}{22,4} = 0,1\, (mol)\)
- Phương trình phản ứng hóa học:
\(CO_{2} + Ba(OH)_{2} \rightarrow BaCO_{3} + H_{2}O\)
2. Dựa vào phương trình phản ứng trên ta nhận thấy:
\(n_{Ba(OH)_{2}} = n_{CO_{2}} = 0,1\, (mol)\)
\(V_{Ba(OH)_{2}} = 200\, ml = 0,2\, (l)\)
\(\Rightarrow C_{M(Ba(OH)_{2})} = \frac{n}{V} = \frac{0,1}{0,2} = 0,5\, M\)
3. Dựa vào phương trình phản ứng trên ta có:
\(n_{BaCO_{3}} = n_{CO_{2}} = 0,1\, mol.\)
\(\Rightarrow m_{BaCO_{3}} = 0,1 . 197 = 19,7g .\)
Xem thêm >>> Lý thuyết và Các dạng bài tập về chủ đề một số oxit quan trọng
Xem thêm >>> Một số axit quan trọng: Lý thuyết và Các dạng bài tập
Bài viết trên đây của DINHNGHIA.VN đã giúp bạn hệ thống hóa kiến thức về chủ đề một số oxit quan trọng. Hy vọng với những thông tin trong bài viết đã hữu ích với bạn trong quá trình học tập. Nếu có bất cứ câu hỏi nào phát sinh liên quan đến chủ đề bài viết một số oxit quan trọng, đừng quên để lại nhận xét bên dưới để chúng mình cùng trao đổi thêm nhé. Chúc bạn luôn học tốt!